炎症研究相关因子之TNF-R1
肿瘤坏死因子受体1(Tumor Necrosis Factor Receptor 1,TNF-R1)是肿瘤坏死因子(TNF)信号通路中的关键膜受体,广泛表达于除红细胞外的几乎所有体细胞表面,尤其在免疫细胞、内皮细胞及实质细胞中高表达。作为介导TNF促炎、促凋亡等核心生物学效应的主要受体,TNF-R1在感染性炎症、自身免疫性炎症、组织损伤与修复等多种生理病理过程中发挥关键调控作用,是炎症研究及相关疾病治疗的重要靶点。
TNF-R1基因定位于人类染色体12p13.31,编码由455个氨基酸残基组成的I型跨膜糖蛋白,相对分子质量约为55 kDa(故又称p55 TNF受体)。其分子结构可分为胞外区、跨膜区和胞内区三部分:胞外区包含4个富含半胱氨酸的重复序列(CRD),是与配体(主要为TNF-α,也可结合淋巴毒素α)特异性结合的核心区域;胞内区含有一个保守的“死亡结构域”(DD),该结构域可通过招募下游衔接蛋白(如TRADD、FADD等)启动信号转导。TNF-R1无需配体诱导即可成同源三聚体,配体结合后会引发受体构象变化,进一步激活下游的炎症和凋亡信号通路,实现对细胞功能的调控。
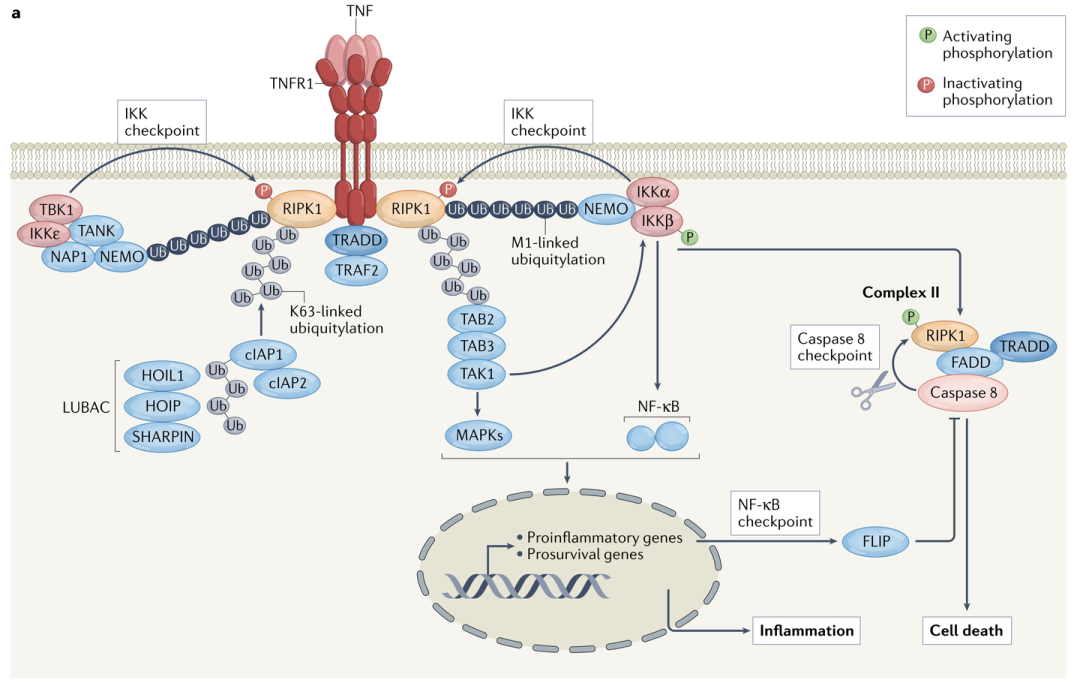
作用:
TNF - R1所介导的信号通路呈现出显著的复杂性,其最终效应(促炎或促凋亡)主要取决于细胞类型、微环境中其他信号分子的存在状况,以及受体激活的强度与持续时间。其中,促炎效应是该信号通路在炎症反应中的核心功能。
(一)促炎效应:启动和放大炎症级联反应
TNF - R1作为炎症反应的关键“启动器”,当机体遭受病原体感染、组织损伤等刺激时,巨噬细胞、淋巴细胞等所分泌的TNF - α会与靶细胞表面的TNF - R1相结合,通过胞内死亡结构域募集TRADD(TNF受体相关死亡域蛋白),进而激活两条至关重要的促炎信号通路。其一为NF - κB(核因子κB)通路。TRADD能够招募TRAF2(TNF受体相关因子2)等分子,借助磷酸化级联反应激活NF - κB,促使其进入细胞核内,对IL - 6、IL - 8、TNF - α等促炎细胞因子以及黏附分子(如ICAM - 1、VCAM - 1)的基因表达进行调控。这些分子可招募并活化中性粒细胞、巨噬细胞等炎症细胞,从而放大炎症反应。其二是MAPK(丝裂原活化蛋白激酶)通路。TRAF2还能够激活JNK、p38等MAPK家族成员,进一步推动促炎细胞因子的转录与分泌,同时对细胞增殖和应激反应加以调控。此外,TNF - R1的激活还能够诱导巨噬细胞释放一氧化氮(NO)、活性氧(ROS)等炎症介质,加重局部组织的炎症损伤。这一过程在败血症、类风湿关节炎等严重炎症性疾病中表现得尤为明显。
(二)促凋亡效应:调控细胞死亡与炎症稳态
当NF - κB通路受到抑制,或者细胞处于应激状态时,TNF - R1会开启促凋亡信号通路。该通路通过清除受损细胞或被病原体感染的细胞来维持机体的稳态,与此同时,凋亡细胞释放的信号还能够调控炎症反应的强度。具体机制如下:TNF - R1与TRADD结合后,若NF - κB通路未被有效激活,TRADD会进一步招募FADD(Fas相关死亡域蛋白)和caspase - 8前体,形成“死亡诱导信号复合物”(DISC),从而激活caspase - 8,进而启动caspase级联反应,最终引发细胞凋亡。此外,TNF - R1介导的凋亡过程还能通过线粒体依赖途径进行放大:caspase - 8被激活后,可切割Bid蛋白,促使线粒体释放细胞色素c,进一步激活caspase - 9和caspase - 3,加速细胞死亡。TNF - R1作为TNF信号通路的核心受体,是衔接炎症刺激与下游病理生理效应的关键节点,其在炎症反应中的调控作用具备重要的生理和病理意义。


 销售咨询
销售咨询